Применяется в технически чистом виде в электротехнической промышленности, а неэлектрорафинированная медь – для производства сплавов.
Руда
- сульфидные руды, горные породы медный колчедан или халькопирит: 60-90% пирита FeS2 и 1-3% меди в виде соединений Cu2S, CuS. До 80% меди получают из сульфидных руд. Cu2O – куприт.
- окисленные руды, из них добывают до 15% Cu (CuO, Cu2O – куприт; CuСO3 Cu(OН)2 – азурит).
- самородная медь встречается примерно на 5%.
90% Cu извлекают пирометаллургическим способом. Около 10% меди путем подвергания бедных руд выщелачиванием – гидрометаллургический способ.
Процесс производства
Технологический процесс пирометаллургического способа производства меди включает следующие стадии (рисунок 1.6):
1) Обогащение руды:
- дробление и размол (до зерен размером 0,05÷0,5 мм);
- флотационное обогащение основано на том, что в пульте несмачивающиеся частицы руды вместе с пузырьками продуваемого воздуха поднимается вверх в виде пены (добавляют масла и другие вещества, образующие на поверхности частиц пленки), а пустая порода смачиваясь вниз.
Полученный концентрат содержит до 10–35% меди;
2) Обжиг в специальных многоходовых вертикальных печах (за счет горения S (CuS, Cu2S и др.), t = 80°) или обжиг в кипящем слое (в кипящем слое 600–700°C CО2 воздуха) → окисление серы и железа (утилизируется 2-х окиcь SO2) – увеличивается в 1,5-2 раза.
3) Получение медного штейна
FeS · Cu2S – в специальных шахтных вертикальных или пламенных отражательных печах:
20–60% Cu, 10-60% Fe и 20-25% S.
с tплавл. ≈ 950-1050 °С. Пустая порода, как шлак;
4) Получение черновой меди – путем продувки жидкого штейна кислородом в горизонтальных и вертикальных конверторах:
Cu2S + O2 = 2Cu + SO2↑
идет на производство кислот, а внизу откладывается черновая медь, которую разливают в чушки или на плиты;
Dконв = 3-4 м, L = 6-10 м, футеровка основная магнезитовым кирпичом.
Рвозд. = 0,8-1,2 атм.
5) Рафинирование меди:
Основной способ электролитический – медь для электротехнической промышленности или загрязненных благородными металлами в электролизных ваннах: происходит растворение анодов (Cu++) и откладывается на катодах. 10-16% Cu2SO4 + 10–16% H2SO4 на получение 1 т Cu – расходуется 250–300 кВт/ч электроэнергии, получают 5 марок М0÷М4 99,0-99,95% Cu. В = 1,2 м, h = 1 м, L = 2,5-3 м, корпус из дерева или бетона, внутри обкладка пластмассой: 20-30 суток – вес катодов из 99,95% Cu ~ 60-90 кг.
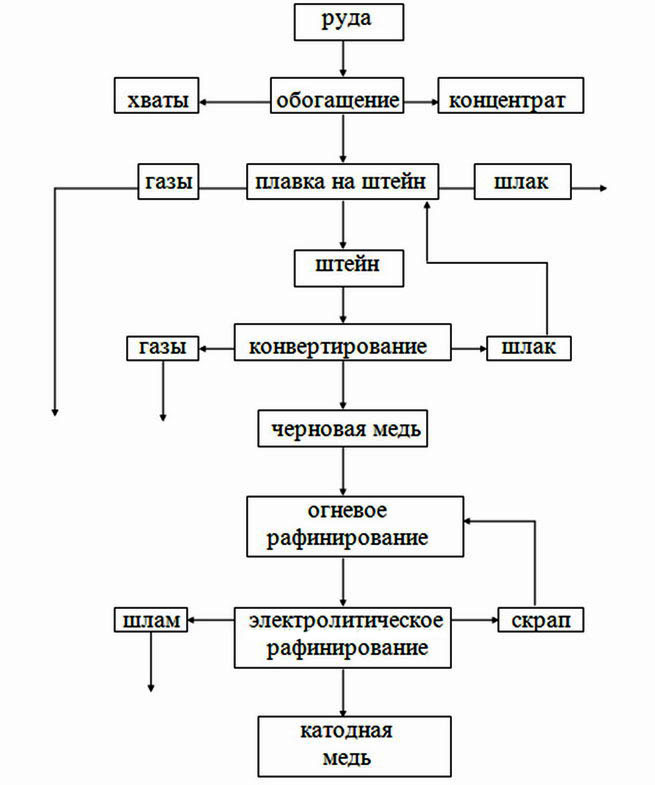
Рисунок 1.6 – Упрощенная схема получения из сульфидных руд пирометаллургическим способом.